الروابط في الجرافيت والماس كلها تساهمية لكنا الاصطفاف البلوري ونوعية الروابط الداخلية بين البلورات نفسها هو المختلف بينها.
الكربون يكون روابط تساهمية احادية في اتجاه واحد حيث يكون التهجين هنا هو 1 sp .
الجرافيت يكون روابط تساهمية أحادية وثنائية حيث تتشارك 3 الكترونات وتدخل المدار المهجن الناتج sp2 وبالتالي تكون الروابط باتجاهين ( ثنائية الابعاد).....في حالة الجرافيت تكون ذرات الكربون مصطفة بشكل يولد حلقات سداسية مسطحة.
اما الألماس فتتكون روابط ثلاثية الابعاد او لنقل ان الروابط بين ذرات الكربون تكون شبكة بلورية وهو ما يعطي هذه الشبكة الثباتية الكبيرة وعدم القابلية للكسر ، ويكون الماس:
-الماس أقوى معدن عرفه الانسان. بينما الجرافيت من اطرى المواد.(عدم وجود شبكة بلورية يجعل طبقات الجرافيت تنزلق فوق بعضها بسلاسة).
-الماس من أقوى عوازل الكهرباء بينما الجرافيت من احسن الموصلات لها.
-بسبب قساوة الماس فهو يعتبر اقوى المواد المخرشة ويستخدم بالات القطع....بينما الجرافيت له من الطرواة ما يجعله يستخدم كمادة تزليق او تشحيم للألات.
وهنا أرفق لكي صور البلورات لكل من الجرافيت والماس:

الجرافيت : تكون الذرات مرتبطة مع بعضها في تشكيل بلوري سداسي Hexagonal ومكونة مع بعضها طبقات الا ان هذه الطبقات تكون مصطفة فوق بعضها بروابط ضعيفة.
الماس: تكون الذرات مرتبطة مع بعضها في تشكيل بلوري رباعي يعرف بـ Tetrahedron وهذا الاصطفاف يسمح بتشكيل روابط قوية بين البلورات الأخرى وفي جميع الاتجهات.
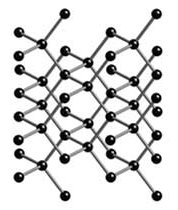
وهذه صورة مصغرة للجرافيت:








